Как именно ФМН и ФАД регулируют белковый метаболизм у молочных коров?
Часть II: Центральная роль рибофлавина в синтезе белка в рубце микроорганизмов и в цикле метионина.
Белковый обмен является одним из важнейших физиологических процессов, определяющих показатели роста, состояние здоровья и выход молочного белка у молочных коров. На молекулярном уровне этот процесс жестко регулируется коферментами, производными рибофлавина,флавинмононуклеотид (FMN) и флавинадениндинуклеотид (FAD)Эти флавины выполняют функцию незаменимых регуляторов окислительно-восстановительного баланса, координируя синтез микробных белков в рубце и метаболизм аминокислот в организме животного.
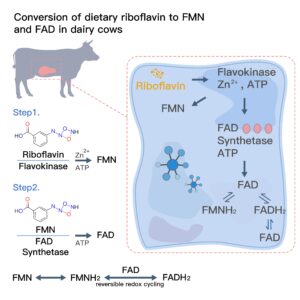
1. Превращение рибофлавина в ФМН и ФАД у молочных коров
Рибофлавин проявляет свою биологическую активность только после превращения в коферментные формы. Это превращение включает два АТФ-зависимых ферментативных этапа:
- Флавокиназа катализирует фосфорилирование рибофлавина с образованием ФМН.
- Впоследствии FAD-синтетаза аденилирует FMN, образуя FAD.
Эффективность этих реакций зависит от энергетической ценности рациона коровы и содержания в нем микроэлементов. Например, цинк действует как активатор флавокиназы, связывая метаболизм рибофлавина с общим минеральным питанием.
Отличительной чертой FMN и FAD является их обратимая окислительно-восстановительная способность.Окисленные формы (FMN, FAD) принимают атомы водорода и электроны, превращаясь в FMNH₂ и FADH₂, а затем возвращаются в окисленное состояние после переноса электронов. Этот цикл обеспечивает непрерывное участие в метаболических реакциях без расхода, что делает флавины идеальными регуляторами ферментативных путей, связанных с белками.
2. Точная регуляция FMN и FAD в белковом метаболизме у крупного рогатого скота
2.1 Важность микробного белка для молочных коров
Микроорганизмы рубца преобразуют азот из корма и небелковый азот (НПН), такой как мочевина, в микробный белок. Этот микробный белок может способствовать 30–50% от общего количества усваиваемого сырого белка доступность белка для молочных коров делает его одним из основных факторов, определяющих эффективность его усвоения.
However, microbial protein synthesis is highly sensitive to coenzyme availability. FMN and FAD function as prosthetic groups for numerous microbial enzymes, including:
- Синтез аминокислот
- Трансаминазы
- Оксидоредуктазы, участвующие в ассимиляции азота
2.2 Роль ФМН и ФАД в активности микробных ферментов
Флавинзависимые ферменты непосредственно участвуют в синтезе аминокислот, таких как аланин и глутамат, которые служат предшественниками для образования пептидов и белков в микробных клетках. Адекватное поступление рибофлавина усиливает синтез ФМН и ФАД, тем самым:
- Повышение активности флавинзависимых ферментов
- Стимулирование роста микроорганизмов и синтеза белка.
- Повышение эффективности преобразования азота из корма.
3. ФАД и метиониновый цикл
3.1 Метионин как лимитирующая аминокислота для синтеза молочного белка
Помимо рубца, белковый обмен у молочных коров регулируется также на уровне метаболизма аминокислот в организме хозяина. Среди незаменимых аминокислот, метионин Метионин часто является первым лимитирующим фактором синтеза молочного белка. Недостаточное поступление метионина связано с Снижение выхода молочного белка на 8–12% у высокопродуктивных молочных коров.
3.2 FAD-зависимая регуляция одноуглеродного метаболизма
ФАД играет ключевую роль в качестве кофермента для метилентетрагидрофолат редуктаза (MTHFR), MTHFR — ключевой фермент в цикле метионина. Он катализирует превращение:
- 5,10-метилентетрагидрофолат → 5-метилтетрагидрофолат
Эта реакция является центральным этапом одноуглеродного метаболизма, обеспечивая стабильный перенос метильных групп. Образующийся 5-метилтетрагидрофолат служит донором метильных групп для реметилирования гомоцистеина в метионин.
4. Синергетическое действие рибофлавина и фолиевой кислоты
Рибофлавин и фолиевая кислота демонстрируют хорошо задокументированную синергию питательных веществ у молочных коров:
- Фолиевая кислота выполняет функцию переносчика одноуглеродных единиц.
- ФАД, получаемый из рибофлавина, обеспечивает активацию и рециркуляцию фолатных коферментов.
При достаточном поступлении обоих питательных веществ эффективность метионинового цикла может повыситься, что приведет к следующим результатам:
- Улучшен баланс аминокислот
- Усиленный синтез молочного белка
- Повышенная метаболическая устойчивость в начале лактации
Эта синергия особенно важна для высокопродуктивных молочных коров, потребность которых в метильных группах и аминокислотах существенно повышена.
Заключение
ФМН и ФАД, биологически активные производные рибофлавина, играют решающую роль в регуляции белкового обмена у молочных коров. Благодаря своему двойному действию на синтез белка в рубце и метиониновый цикл хозяина, эти флавиновые коферменты повышают эффективность использования азота, поддерживают синтез молочного белка и улучшают общие показатели продуктивности.
References
Historical Discovery and Early Research Literature (1879-1935)
1. Blyth, A. W. (1879). On the yellow pigment of milk whey (lactochrome). Journal of the Chemical Society, Transactions, 35, 532-535. https://doi.org/10.1039/CT8793500530
2. Chick, H., & Roscoe, M. H. (1928). The dual nature of water-soluble vitamin B. II. The effect upon young rats of vitamin B2 deficiency and a method for the biological assay of vitamin B2. Biochemical Journal, 22, 790-799. https://doi.org/10.1042/bj0220790
3. Kuhn, R., & Wendt, H. (1933). Über Lactoflavin, ein Vitamin B2-haltiges Pigment aus Milch. Berichte der Deutschen Chemischen Gesellschaft, 66, 1262-1267. https://doi.org/10.1002/cber.19330660823
4. Karrer, P., et al. (1933). Über die Isolierung von Lactoflavin in reiner Form aus Milch. Helvetica Chimica Acta, 16, 1059-1064. https://doi.org/10.1002/hlca.19330160327
5. Kuhn, R., et al. (1933). Über Ovoflavin, ein Vitamin B2-haltiges Pigment aus Eiern. Berichte der Deutschen Chemischen Gesellschaft, 66, 1301-1308. https://doi.org/10.1002/cber.19330660828
6. Kuhn, R., et al. (1935). Über die Struktur des Lactoflavins (Riboflavin). Berichte der Deutschen Chemischen Gesellschaft, 68, 2067-2074. https://doi.org/10.1002/cber.19350681226
7. Kuhn, R., et al. (1935). Über die Synthese des Riboflavins (Vitamin B2). Angewandte Chemie, 48, 177-182. https://doi.org/10.1002/ange.19350480402
8. McCormick, D. B., & Greene, T. J. (2012). The discovery and characterization of riboflavin. Annals of Nutrition & Metabolism, 61, 224-230. https://doi.org/10.1159/000343111



