Como o FMN e o FAD regulam precisamente o metabolismo proteico em vacas leiteiras?
Parte II: O Papel Central da Riboflavina na Síntese de Proteína Microbiana do Rúmen e no Ciclo da Metionina
O metabolismo de proteínas é um dos processos fisiológicos mais críticos que determinam o desempenho de crescimento, o estado de saúde e a produção de proteína do leite em vacas leiteiras. Em nível molecular, esse processo é rigorosamente regulado por coenzimas derivadas da riboflavina -mononucleotídeo de flavina (FMN) e dinucleotídeo de flavina adenina (FAD)Essas flavinas funcionam como reguladores redox indispensáveis, coordenando a síntese de proteínas microbianas no rúmen e o metabolismo de aminoácidos no animal hospedeiro.
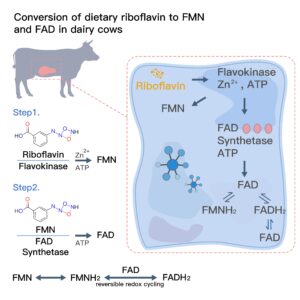
1. Conversão de riboflavina em FMN e FAD em vacas leiteiras
A riboflavina exerce sua atividade biológica somente após ser convertida em suas formas de coenzima. Essa conversão envolve duas etapas enzimáticas dependentes de ATP:
- A flavocinase catalisa a fosforilação da riboflavina para formar FMN.
- A FAD sintetase adenila subsequentemente o FMN para produzir FAD.
A eficiência dessas reações é influenciada pelo fornecimento de energia na dieta da vaca e pelo seu estado nutricional em relação aos oligoelementos. Por exemplo, o zinco atua como um ativador da flavocinase, ligando o metabolismo da riboflavina à nutrição mineral geral.
Uma característica definidora de FMN e FAD é a sua capacidade redox reversível.As formas oxidadas (FMN, FAD) aceitam átomos de hidrogênio e elétrons para se tornarem FMNH₂ e FADH₂, e então retornam aos seus estados oxidados após a transferência de elétrons. Esse ciclo permite a participação contínua em reações metabólicas sem serem consumidas, tornando as flavinas reguladoras ideais de vias enzimáticas relacionadas a proteínas.
2. Regulação precisa de FMN e FAD no metabolismo de proteínas em bovinos
2.1 Importância da proteína microbiana para vacas leiteiras
Os microrganismos do rúmen convertem o nitrogênio da dieta e o nitrogênio não proteico (NNP), como a ureia, em proteína microbiana. Essa proteína microbiana pode contribuir 30–50% da proteína bruta absorvível total disponível para vacas leiteiras, tornando-se um importante determinante da eficiência de utilização de proteínas.
However, microbial protein synthesis is highly sensitive to coenzyme availability. FMN and FAD function as prosthetic groups for numerous microbial enzymes, including:
- Sintetasas de aminoácidos
- Transaminases
- Oxidoredutases envolvidas na assimilação de nitrogênio
2.2 Papel do FMN e do FAD na atividade enzimática microbiana
As enzimas dependentes de flavina estão diretamente envolvidas na síntese de aminoácidos como alanina e glutamato, que servem como precursores para a formação de peptídeos e proteínas dentro das células microbianas. O suprimento adequado de riboflavina aumenta a síntese de FMN e FAD, resultando em:
- Aumentar a atividade de enzimas flavina-dependentes
- Promover o crescimento microbiano e a síntese de proteínas.
- Melhorar a eficiência de conversão do nitrogênio dietético
3. FAD e o Ciclo da Metionina
3.1 Metionina como aminoácido limitante para a síntese de proteína do leite
Além do rúmen, o metabolismo proteico em vacas leiteiras é ainda mais regulado no nível do metabolismo de aminoácidos do hospedeiro. Entre os aminoácidos essenciais, metionina A insuficiência de metionina é frequentemente o primeiro fator limitante para a síntese de proteínas do leite. O fornecimento insuficiente de metionina tem sido associado a uma Redução de 8 a 12% no rendimento de proteína do leite em vacas leiteiras de alta produção.
3.2 Regulação do metabolismo de um carbono dependente de FAD
O FAD desempenha um papel fundamental como coenzima para metilenotetraidrofolato redutase (MTHFR), uma enzima chave no ciclo da metionina. A MTHFR catalisa a conversão de:
- 5,10-metilenotetraidrofolato → 5-metiltetraidrofolato 保存翻译
Essa reação é a etapa central do metabolismo de um carbono, garantindo a transferência estável de grupos metil. O 5-metiltetraidrofolato resultante serve como doador de metil para a remetilação da homocisteína em metionina.
4. Efeitos sinérgicos da riboflavina e do ácido fólico
A riboflavina e o ácido fólico apresentam uma sinergia nutricional bem documentada em vacas leiteiras:
- O ácido fólico funciona como transportador de unidades de um carbono.
- O FAD, derivado da riboflavina, garante a ativação e a reciclagem das coenzimas do folato.
Quando ambos os nutrientes são fornecidos adequadamente, a eficiência do ciclo da metionina pode aumentar, resultando em:
- Melhoria do equilíbrio de aminoácidos
- Síntese aprimorada de proteína do leite
- Melhor resiliência metabólica no início da lactação
Essa sinergia é particularmente importante para vacas leiteiras de alta produção, cuja demanda por grupos metil e aminoácidos é substancialmente elevada.
Conclusão
FMN e FAD, derivados biologicamente ativos da riboflavina, desempenham um papel decisivo na regulação do metabolismo proteico em vacas leiteiras. Através de sua dupla ação na síntese de proteína microbiana no rúmen e no ciclo da metionina do hospedeiro, essas coenzimas flavínicas aumentam a eficiência da utilização de nitrogênio, auxiliam na síntese de proteína do leite e melhoram o desempenho produtivo geral.
References
Historical Discovery and Early Research Literature (1879-1935)
1. Blyth, A. W. (1879). On the yellow pigment of milk whey (lactochrome). Journal of the Chemical Society, Transactions, 35, 532-535. https://doi.org/10.1039/CT8793500530
2. Chick, H., & Roscoe, M. H. (1928). The dual nature of water-soluble vitamin B. II. The effect upon young rats of vitamin B2 deficiency and a method for the biological assay of vitamin B2. Biochemical Journal, 22, 790-799. https://doi.org/10.1042/bj0220790
3. Kuhn, R., & Wendt, H. (1933). Über Lactoflavin, ein Vitamin B2-haltiges Pigment aus Milch. Berichte der Deutschen Chemischen Gesellschaft, 66, 1262-1267. https://doi.org/10.1002/cber.19330660823
4. Karrer, P., et al. (1933). Über die Isolierung von Lactoflavin in reiner Form aus Milch. Helvetica Chimica Acta, 16, 1059-1064. https://doi.org/10.1002/hlca.19330160327
5. Kuhn, R., et al. (1933). Über Ovoflavin, ein Vitamin B2-haltiges Pigment aus Eiern. Berichte der Deutschen Chemischen Gesellschaft, 66, 1301-1308. https://doi.org/10.1002/cber.19330660828
6. Kuhn, R., et al. (1935). Über die Struktur des Lactoflavins (Riboflavin). Berichte der Deutschen Chemischen Gesellschaft, 68, 2067-2074. https://doi.org/10.1002/cber.19350681226
7. Kuhn, R., et al. (1935). Über die Synthese des Riboflavins (Vitamin B2). Angewandte Chemie, 48, 177-182. https://doi.org/10.1002/ange.19350480402
8. McCormick, D. B., & Greene, T. J. (2012). The discovery and characterization of riboflavin. Annals of Nutrition & Metabolism, 61, 224-230. https://doi.org/10.1159/000343111



