Comment le FMN et le FAD régulent-ils précisément le métabolisme des protéines chez les vaches laitières ?
Partie II : Le rôle central de la riboflavine dans la synthèse des protéines microbiennes du rumen et le cycle de la méthionine
Le métabolisme des protéines est l'un des processus physiologiques les plus importants qui déterminent la croissance, l'état de santé et la production de protéines laitières chez les vaches. Au niveau moléculaire, ce processus est étroitement régulé par des coenzymes dérivés de la riboflavine :mononucléotide de flavine (FMN) et dinucléotide de flavine adénine (FAD)Ces flavines jouent le rôle de régulateurs redox indispensables, coordonnant la synthèse des protéines microbiennes dans le rumen et le métabolisme des acides aminés chez l'animal hôte.
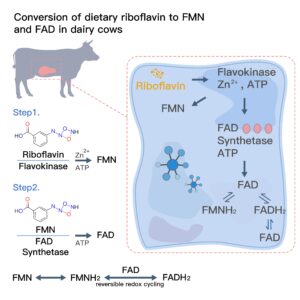
1. Conversion de la riboflavine en FMN et FAD chez les vaches laitières
La riboflavine n'exerce son activité biologique qu'après avoir été convertie en ses formes coenzymatiques. Cette conversion implique deux étapes enzymatiques dépendantes de l'ATP :
- La flavokinase catalyse la phosphorylation de la riboflavine pour former la FMN
- La FAD synthétase adényle ensuite la FMN pour produire du FAD.
L’efficacité de ces réactions dépend de l’apport énergétique et du statut en oligo-éléments de l’alimentation de la vache. Par exemple, le zinc agit comme activateur de la flavokinase, reliant ainsi le métabolisme de la riboflavine à la nutrition minérale globale.
Une caractéristique déterminante de FMN et FAD est leur capacité redox réversible.Les formes oxydées (FMN, FAD) acceptent des atomes d'hydrogène et des électrons pour devenir FMNH₂ et FADH₂, puis retournent à leur état oxydé après transfert d'électrons. Ce cycle permet une participation continue aux réactions métaboliques sans consommation, faisant des flavines des régulateurs idéaux des voies enzymatiques liées aux protéines.
2. Régulation précise du FMN et du FAD sur le métabolisme des protéines chez les bovins
2.1 Importance des protéines microbiennes pour les vaches laitières
Les micro-organismes du rumen transforment l'azote alimentaire et l'azote non protéique (NPN), comme l'urée, en protéines microbiennes. Ces protéines microbiennes peuvent contribuer 30 à 50 % des protéines brutes absorbables totales disponible pour les vaches laitières, ce qui en fait un facteur déterminant de l'efficacité d'utilisation des protéines.
However, microbial protein synthesis is highly sensitive to coenzyme availability. FMN and FAD function as prosthetic groups for numerous microbial enzymes, including:
- synthases d'acides aminés
- Transaminases
- Oxydoréductases impliquées dans l'assimilation de l'azote
2.2 Rôle du FMN et du FAD dans l'activité enzymatique microbienne
Les enzymes flavine-dépendantes participent directement à la synthèse d'acides aminés tels que l'alanine et le glutamate, précurseurs de la formation de peptides et de protéines au sein des cellules microbiennes. Un apport suffisant en riboflavine stimule la synthèse de FMN et de FAD, et par conséquent :
- Augmenter l'activité des enzymes flavine-dépendantes
- Favoriser la croissance microbienne et la synthèse protéique
- Améliorer l'efficacité de conversion de l'azote alimentaire
3. Le FAD et le cycle de la méthionine
3.1 La méthionine comme acide aminé limitant la synthèse des protéines du lait
Au-delà du rumen, le métabolisme des protéines chez les vaches laitières est également régulé au niveau du métabolisme des acides aminés de l'hôte. Parmi les acides aminés essentiels, méthionine Le premier facteur limitant la synthèse des protéines du lait est souvent la carence en méthionine. Un apport insuffisant en méthionine a été associé à réduction de 8 à 12 % du rendement en protéines du lait chez les vaches laitières à haut rendement.
3.2 Régulation du métabolisme du carbone à un atome dépendante du FAD
Le FAD joue un rôle essentiel en tant que coenzyme pour méthylènetétrahydrofolate réductase (MTHFR), une enzyme clé du cycle de la méthionine. La MTHFR catalyse la conversion de :
- 5,10-méthylènetétrahydrofolate → 5-méthyltétrahydrofolate
Cette réaction est l'étape centrale du métabolisme du carbone à un atome, assurant le transfert stable des groupements méthyle. Le 5-méthyltétrahydrofolate ainsi formé sert de donneur de méthyle pour la reméthylation de l'homocystéine en méthionine.
4. Effets synergiques de la riboflavine et de l'acide folique
La riboflavine et l'acide folique présentent une synergie nutritionnelle bien documentée chez les vaches laitières :
- L'acide folique agit comme transporteur d'unités à un carbone
- Le FAD, dérivé de la riboflavine, assure l'activation et le recyclage des coenzymes folates.
Lorsque les deux nutriments sont apportés en quantité suffisante, l'efficacité du cycle de la méthionine peut augmenter, ce qui entraîne :
- Amélioration de l'équilibre des acides aminés
- Synthèse améliorée des protéines du lait
- Meilleure résilience métabolique en début de lactation
Cette synergie est particulièrement importante pour les vaches laitières à haut rendement, dont les besoins en groupes méthyle et en acides aminés sont considérablement plus élevés.
Conclusion
La FMN et la FAD, dérivés biologiquement actifs de la riboflavine, jouent un rôle déterminant dans la régulation du métabolisme protéique chez les vaches laitières. Par leur double action sur la synthèse des protéines microbiennes du rumen et le cycle de la méthionine de l'hôte, ces coenzymes flaviniques améliorent l'efficacité d'utilisation de l'azote, favorisent la synthèse des protéines du lait et optimisent les performances de production.
References
Historical Discovery and Early Research Literature (1879-1935)
1. Blyth, A. W. (1879). On the yellow pigment of milk whey (lactochrome). Journal of the Chemical Society, Transactions, 35, 532-535. https://doi.org/10.1039/CT8793500530
2. Chick, H., & Roscoe, M. H. (1928). The dual nature of water-soluble vitamin B. II. The effect upon young rats of vitamin B2 deficiency and a method for the biological assay of vitamin B2. Biochemical Journal, 22, 790-799. https://doi.org/10.1042/bj0220790
3. Kuhn, R., & Wendt, H. (1933). Über Lactoflavin, ein Vitamin B2-haltiges Pigment aus Milch. Berichte der Deutschen Chemischen Gesellschaft, 66, 1262-1267. https://doi.org/10.1002/cber.19330660823
4. Karrer, P., et al. (1933). Über die Isolierung von Lactoflavin in reiner Form aus Milch. Helvetica Chimica Acta, 16, 1059-1064. https://doi.org/10.1002/hlca.19330160327
5. Kuhn, R., et al. (1933). Über Ovoflavin, ein Vitamin B2-haltiges Pigment aus Eiern. Berichte der Deutschen Chemischen Gesellschaft, 66, 1301-1308. https://doi.org/10.1002/cber.19330660828
6. Kuhn, R., et al. (1935). Über die Struktur des Lactoflavins (Riboflavin). Berichte der Deutschen Chemischen Gesellschaft, 68, 2067-2074. https://doi.org/10.1002/cber.19350681226
7. Kuhn, R., et al. (1935). Über die Synthese des Riboflavins (Vitamin B2). Angewandte Chemie, 48, 177-182. https://doi.org/10.1002/ange.19350480402
8. McCormick, D. B., & Greene, T. J. (2012). The discovery and characterization of riboflavin. Annals of Nutrition & Metabolism, 61, 224-230. https://doi.org/10.1159/000343111



