¿Cómo FMN y FAD regulan con precisión el metabolismo de proteínas en las vacas lecheras?
Parte II: El papel central de la riboflavina en la síntesis de proteínas microbianas del rumen y el ciclo de la metionina
El metabolismo proteico es uno de los procesos fisiológicos más críticos que determinan el rendimiento del crecimiento, el estado de salud y la producción de proteína láctea en las vacas lecheras. A nivel molecular, este proceso está estrechamente regulado por las coenzimas derivadas de la riboflavina:mononucleótido de flavina (FMN) y dinucleótido de flavina y adenina (FAD)Estas flavinas funcionan como reguladores redox indispensables, coordinando la síntesis de proteínas microbianas en el rumen y el metabolismo de aminoácidos en el animal huésped.
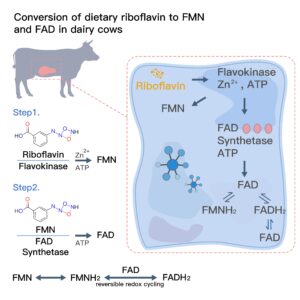
1. Conversión de riboflavina en FMN y FAD en vacas lecheras
La riboflavina ejerce su actividad biológica solo tras ser convertida en sus formas coenzimáticas. Esta conversión implica dos pasos enzimáticos dependientes de ATP:
- La flavoquinasa cataliza la fosforilación de la riboflavina para formar FMN.
- La FAD sintetasa posteriormente adenila FMN para producir FAD.
La eficiencia de estas reacciones depende del aporte energético de la dieta de la vaca y del estado de oligoelementos. Por ejemplo, el zinc actúa como activador de la flavoquinasa, vinculando el metabolismo de la riboflavina con la nutrición mineral general.
Una característica definitoria de FMN y FAD es su capacidad redox reversible.Las formas oxidadas (FMN, FAD) aceptan átomos de hidrógeno y electrones para convertirse en FMNH₂ y FADH₂, y luego regresan a sus estados oxidados tras la transferencia de electrones. Este ciclo permite la participación continua en reacciones metabólicas sin ser consumidas, lo que convierte a las flavinas en reguladores ideales de las vías enzimáticas relacionadas con las proteínas.
2. Regulación precisa de FMN y FAD sobre el metabolismo proteico en el ganado
2.1 Importancia de la proteína microbiana para las vacas lecheras
Los microorganismos del rumen convierten el nitrógeno de la dieta y el nitrógeno no proteico (NNP), como la urea, en proteína microbiana. Esta proteína microbiana puede contribuir 30–50% de la proteína cruda total absorbible disponible para las vacas lecheras, lo que lo convierte en un determinante importante de la eficiencia de utilización de proteínas.
However, microbial protein synthesis is highly sensitive to coenzyme availability. FMN and FAD function as prosthetic groups for numerous microbial enzymes, including:
- Aminoácido sintases
- Transaminasas
- Oxidorreductasas implicadas en la asimilación de nitrógeno
2.2 Papel de FMN y FAD en la actividad enzimática microbiana
Las enzimas dependientes de flavina participan directamente en la síntesis de aminoácidos como la alanina y el glutamato, que sirven como precursores para la formación de péptidos y proteínas en las células microbianas. Un aporte adecuado de riboflavina potencia la síntesis de FMN y FAD, lo que permite:
- Aumento de la actividad de las enzimas dependientes de flavina
- Promoción del crecimiento microbiano y la síntesis de proteínas.
- Mejora de la eficiencia de conversión del nitrógeno dietético
3. FAD y el ciclo de la metionina
3.1 La metionina como aminoácido limitante para la síntesis de proteínas de la leche
Más allá del rumen, el metabolismo proteico en las vacas lecheras se regula aún más a nivel del metabolismo de aminoácidos del huésped. Entre los aminoácidos esenciales, metionina es a menudo el primer factor limitante para la síntesis de proteínas de la leche. Un aporte insuficiente de metionina se ha asociado con una Reducción del 8 al 12 % en el rendimiento de proteína de la leche en vacas lecheras de alta producción.
3.2 Regulación del metabolismo de un carbono dependiente de FAD
El FAD desempeña un papel fundamental como coenzima para metilentetrahidrofolato reductasa (MTHFR), una enzima clave en el ciclo de la metionina. La MTHFR cataliza la conversión de:
- 5,10-metilentetrahidrofolato → 5-metiltetrahidrofolato
Esta reacción es el paso central del metabolismo de un carbono, asegurando la transferencia estable de grupos metilo. El 5-metiltetrahidrofolato resultante actúa como donante de metilo para la remetilación de la homocisteína a metionina.
4. Efectos sinérgicos de la riboflavina y el ácido fólico
La riboflavina y el ácido fólico muestran una sinergia nutricional bien documentada en las vacas lecheras:
- El ácido fólico funciona como transportador de unidades de un carbono.
- El FAD, derivado de la riboflavina, asegura la activación y el reciclaje de las coenzimas del folato.
Cuando ambos nutrientes se suministran adecuadamente, la eficiencia del ciclo de la metionina puede aumentar, dando como resultado:
- Equilibrio mejorado de aminoácidos
- Síntesis mejorada de proteínas de la leche
- Mejor resiliencia metabólica en la lactancia temprana
Esta sinergia es particularmente importante para las vacas lecheras de alto rendimiento, cuya demanda de grupos metilo y aminoácidos es sustancialmente elevada.
Conclusión
FMN y FAD, derivados biológicamente activos de la riboflavina, desempeñan un papel decisivo en la regulación del metabolismo proteico en las vacas lecheras. Gracias a su doble acción en la síntesis de proteínas microbianas del rumen y el ciclo de la metionina del huésped, estas coenzimas de flavina mejoran la eficiencia de la utilización del nitrógeno, favorecen la síntesis de proteínas de la leche y mejoran el rendimiento productivo general.
References
Historical Discovery and Early Research Literature (1879-1935)
1. Blyth, A. W. (1879). On the yellow pigment of milk whey (lactochrome). Journal of the Chemical Society, Transactions, 35, 532-535. https://doi.org/10.1039/CT8793500530
2. Chick, H., & Roscoe, M. H. (1928). The dual nature of water-soluble vitamin B. II. The effect upon young rats of vitamin B2 deficiency and a method for the biological assay of vitamin B2. Biochemical Journal, 22, 790-799. https://doi.org/10.1042/bj0220790
3. Kuhn, R., & Wendt, H. (1933). Über Lactoflavin, ein Vitamin B2-haltiges Pigment aus Milch. Berichte der Deutschen Chemischen Gesellschaft, 66, 1262-1267. https://doi.org/10.1002/cber.19330660823
4. Karrer, P., et al. (1933). Über die Isolierung von Lactoflavin in reiner Form aus Milch. Helvetica Chimica Acta, 16, 1059-1064. https://doi.org/10.1002/hlca.19330160327
5. Kuhn, R., et al. (1933). Über Ovoflavin, ein Vitamin B2-haltiges Pigment aus Eiern. Berichte der Deutschen Chemischen Gesellschaft, 66, 1301-1308. https://doi.org/10.1002/cber.19330660828
6. Kuhn, R., et al. (1935). Über die Struktur des Lactoflavins (Riboflavin). Berichte der Deutschen Chemischen Gesellschaft, 68, 2067-2074. https://doi.org/10.1002/cber.19350681226
7. Kuhn, R., et al. (1935). Über die Synthese des Riboflavins (Vitamin B2). Angewandte Chemie, 48, 177-182. https://doi.org/10.1002/ange.19350480402
8. McCormick, D. B., & Greene, T. J. (2012). The discovery and characterization of riboflavin. Annals of Nutrition & Metabolism, 61, 224-230. https://doi.org/10.1159/000343111



